828号令“倒逼”产业升级!中小药企的春天来了!
2026 年1月27日,国务院正式发布《中华人民共和国药品管理法实施条例》(国令第828号),明确自5月15日起施行。此前1个月,《生物医学新技术临床研究和临床转化应用管理条例》(818 号令)已释放管技术信号,如今 828 号令聚焦管药品,中国生物医药“药+术”双轨监管架构正式闭环。对于企业而言,模糊试探已成过去,合规破局才是未来!——中欧医药中心帮你踩准双轨节奏
818vs828:
一表看懂双轨监管逻辑
很多从业者疑惑:为何国家短期内连发两道重磅令?核心是“清场不合规,加速真创新”。818号令圈定医院端技术的合规边界,828号令明确企业端药品的发展路径,两者互补形成产业规范闭环,具体差异如下: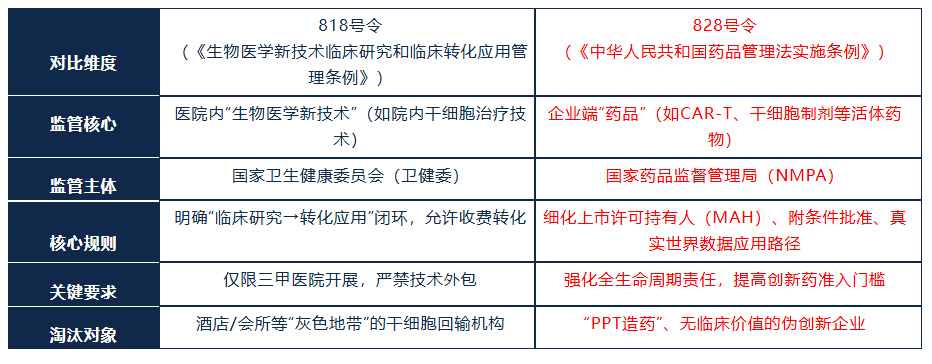
828号令三大关键变革:
企业必须关注的生存法则
828号令并非简单加门槛,而是为真正有创新力的企业开辟快车道。结合条例内容与产业实践,这三大变革直接决定企业未来走向,而中欧医药中心已针对性备好解决方案:
1.MAH制度紧箍咒升级:从甩手掌柜到全周期负责人
新版条例强化上市许可持有人(MAH)的全生命周期责任——以前企业“只研发不管生产销售”的模式彻底行不通,委托生产(CMO)门槛大幅提高,必须具备极强的质量管理能力(QMS)才能获得代工资格。
2.附条件批准常态化:创新药提前上市的机遇与风险
对于晚期癌症等无有效治疗手段的疾病,828号令明确:企业无需等三期临床全部完成,只要二期数据足够扎实,即可申请附条件上市;但上市后必须补做临床,否则将被撤销批文。这对细胞/基因治疗企业而言,是提前变现的重大利好,但也倒逼企业必须有真材实料。
3.真实世界数据(RWE)法定化:打通“临床研究→药品注册”闭环
此前医院开展的IIT(研究者发起的临床研究)数据,药监局多不认可;如今828号令明确:只要数据符合“真实、完整、可溯源”标准(如符合《真实世界证据支持药物研发与审评的指导原则》),IIT数据可直接用于药品注册(IND/NDA)。这意味着企业可通过低成本IIT试错再推进高估值药品上市,形成商业闭环。
中欧医药中心:
828号令下的全链条合规转化生态赋能者
828号令5月15日正式施行,留给企业的准备时间不足4个月。结合双轨监管要求,企业需从三方面行动:
重新评估管线(pipeline):通用型产品(如通用CAR-T)建议走828药品路(天花板高),自体型产品或资金有限企业可先走818技术路(与三甲医院绑定存活)。
恶补数据合规:828号令对数据造假的处罚是“顶格罚款+行业禁入”,企业需建立ALCOA+C原则(可追溯、清晰、同步、原始、准确+完整)的数据系统。中欧可协助搭建符合标准的数据管理平台,开展员工合规培训。
聚焦临床价值:无论是818还是828,核心都指向解决未满足的临床需求,有技术但不知治什么病的企业将被双重淘汰。
企业应对指南:
4个月窗口期,中欧陪你踩准节奏
中欧医药中心依托“基础研究-转化医学-企业引育-国际合作”四大层级创新体系,以300㎡GMP洁净车间、2670㎡中试服务场地、标准化5A级细胞库及AI驱动的ATMP全链条智能化平台为硬件支撑,联动深圳市人民医院、北京协和医院等三甲临床资源与勃林格殷格翰、Cytiva等国际伙伴,构建了适配828号令要求的全周期解决方案,助力孵化企业在“合规竞速”中实现从管线研发到全球注册的高效跃迁,成为828号令下企业破解合规痛点、抢占创新先机的核心生态枢纽。
引用来源:
1.国务院官网:《中华人民共和国药品管理法实施条例》(国令第828号),2026年1月27日
2.“细胞智慧百科”公众号:《重磅818号令后又来828号令:谁在“清场”中出局,谁在“合规”中暴富》,2026年1月28日
3.国家药监局:《真实世界证据支持药物研发与审评的指导原则》(现行有效)

0755-66880601
深圳市罗湖区清水河三路7号中海慧智大厦


